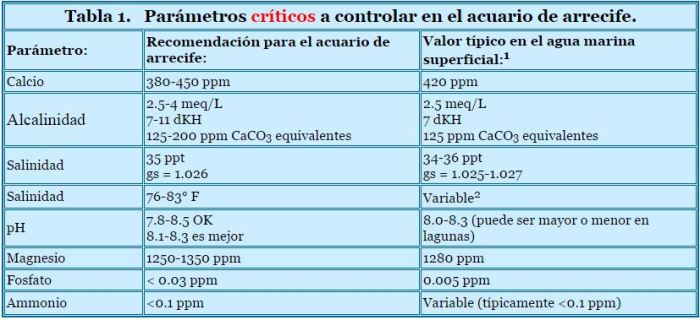
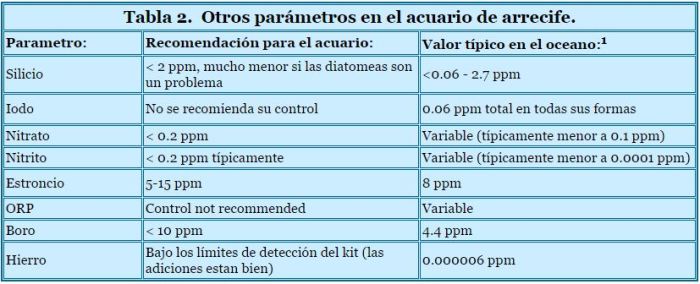
Los acuaristas a menudo preguntan qué parámetros del agua tener para lograr el éxito en un acuario de arrecife. Este artículo reune esas recomendaciones en un solo lugar, se los muestra en tablas, así como muestra los niveles correspondientes en el agua de mar natural.
Calcio
Muchos corales usan calcio para formar sus esqueletos, que están compuestos principalmente de carbonato de calcio. Los corales obtienen mucho del calcio para este proceso del agua que los rodea. Consecuentemente, el calcio es agotado en un acuario albergando corales de rápido crecimiento, alga calcárea roja, Tridacnas y Halimeda. Conforme el calcio cae por debajo de 360 ppm, se hace progresivamente más difícil para los corales colectar suficiente calcio, deteniendo su crecimiento.
Mantener el nivel de calcio es uno de los aspectos más importantes del mantenimiento de acuarios de arrecife. La mayoría de los acuaristas tratan de mantener niveles cercanos a los niveles naturales en su acuario(~420 ppm). El incrementar la concentraciones de calcio por encima de los niveles naturales no parece aumentar la calcificación (i.e., el crecimiento del esqueleto) en la mayoría de los corales. Experimentos con Stylophora pistillata, por ejemplo, mostraron que niveles bajos de calcio limitan la calcificación, pero que niveles arriba de 360 ppm no la incrementan. Exactamente por qué pasa esto se detalló en un artículo previo acerca de los mecanimos moleculares.
Por estas razones, sugiero que los acuaristas mantengan niveles de calcio entre 380 y 450 ppm. También sugiero el usar un, sistema balanceado de adición de alkalinidad y calcio. para sus rutinas de mantenimiento. El más popular de estos métodos balanceados incluye el uso de agua de cal (kalkwasser), reactores de carbonato de calcio/dióxido de carbono, y los sistemas de aditivos de dos partes.
Si el calcio se agota y necesita incrementarse significativamente, tales sistemas balanceados no son buena opción ya que elevarán demasiado la alcalinidad. En tales casos, agregar, cloruro de calcio es un buen método de elevar el calcio.
Alcalinidad
Al igual que el calcio, muchos corales usan «alcalinidad» para construir sus esqueletos, que están compuestos de carbonato de calcio. Generalmente se cree que los corales. toman bicarbonato, y lo convierten en carbonato para formar sus esqueletos de carbonato de calcio. Ese proceso de conversión se muestra como:
HCO3– à CO3— + H+
Bicarbonat0 à Carbonato + ácido
Para asegurarse que los corales tiene una dotación de bicarbonato suficiente para la calcificación, los acuaristas podrían medir directamente el bicarbonato. Sin embargo, diseñar una prueba para bicarbonatos es un poco más complicado que una para alcalinidad. En consecuencia, el uso de la alcalinidad como una medida alternativa para bicarbonato esta fuertemente arraigado en la afición.
Así que, ¿qué es alcalinidad? Alcalinidad en el acuario marino es simplemente una medida de la cantidad de ácido requerida para disminuir el pH alrededor de 4.5, donde todo el bicarbonato se convierte en ácido carbónico así:
HCO3– + H+ à H2CO3
En el agua de mar normal, o la del acuario marino, el ión bicarbonato domina a otros iones que contribuyen a la alcalinidad, así que conocer la cantidad de H+ que se necesita para bajar el pH a 4.5 es lo mismo que saber cuanto bicarbonato está presente. Los acuaristas por lo tanto han hallado conveniente usar la alcalinidad como una medida alternativa de bicarbonatos.
Un problema importante con esta medida alternativa es que algunas mezclas de sal artificial como la de Seachem contienen concentraciones elevadas de borato. Mientras el borato está naturalmente en niveles bajos contribuye a la la estabilidad del pH, pero demasiado interfiere con la relación normal entre bicarbonato y alcalinidad y los acuarios usando esta mezcla deben de tomar esta diferencia en cuenta cuando determinen el nivel de alcalinidad apropiado.
A diferencia de la concentración de calcio, se cree ampliamente que ciertos organismos calcifican más rápidamente a niveles de alcalinidad más elevados que los del agua de mar. Este resultado también se ha demostrado en la literatura científica, que ha determinado que agregar bicarbonato al agua de mar incrementa la tasa de calcificación de Porites. En este caso, doblar la tasa de bicarbonato, elevó la tasa de calcificación al doble. La toma de bicarbonato parece ser limitante en muchos corales. Esto podría deberse parcialmente al hecho de que ambos, fotosíntesis y calcificación están compitiendo por bicarbonatos, y que la concentración de bicarbonato externa no es suficientemente elevada para comenzar (con respecto a, por ejemplo, la concentración de calcio).
Por estas razones, el mantener la alcalinidad es un aspecto crítico del mantenimiento de acuarios de arrecife. En la ausencia de suplementación, la alcalinidad caerá rápidamente conforme los corales usan lo que se encuentre presente en el agua. La mayoría de los acuaristas tratan de mantener los niveles iguales o ligeramente arriba de lo que se encuentra en el agua de mar, aunque exactamente qué niveles tratan de obtener los acuaristas depende de las metas en su acuario. Aquellos que quieran un crecimiento del esqueleto más rápido, por ejemplo, a menudo forzan las cosas en su acuario hacia niveles elevados. Sugiero que los acuaristas mantengan los niveles entre 2.5 y 4 meq/L (7-11 dKH, equivalente a 125-200 ppm de Ca), aunque niveles mayores son aceptables mientras no bajen el nivel de calcio.
Niveles de alcalinidad mayores a los del agua de mar incrementan la precipitación abiótica de calcio sobre objetos como calefactores e impelers de bombas. Esta precipitación no sólo desperdicia el calcio y la alcalinidad que los acuaristas agregan con tanto cuidado, sino que también incrementan los requerimientos para el mantenimiento del equipo. Cuando una alcalinidad elevada esta provocando esta precipitación, también puede bajar el nivel de calcio. Un nivel elevado de alcalinidad puede por tanto crear consecuencias indeseables.
Sugiero que los acuaristas usen un sistema balanceado de adición de alkalinidad y calcio de algún tipo para sus rutinas de mantenimiento. El más popular de estos métodos balanceados incluye el uso de agua de cal (kalkwasser), reactores de carbonato de calcio/dióxido de carbono, y los sistemas de aditivos de dos partes.
Para correciones rápidas de alcalinidad, los acuaristas pueden usar simplemente bicarbonato de sodio con buen efecto.
Los acuaristas gastan una considerable cantidad de tiempo y esfuerzo preocupándose, e intentando resolver, problemas aparentes con el pH de su acuario. Algo de este esfuerzo ciertamente es justificado, ya que verdaderos problemas de pH pueden conducir a una pobre salud en los animales. Sin embargo, en muchos casos, el único problema con el pH es su medición o su interpretación.
Varios factores hacen monitorear el pH del acuario marino importante. Uno es que los organismos acuáticos prosperan sólo a un rango particular de pH, que varia de organismo a organismo. Es por tanto difícil justificar el argumento de que un rango de pH es «óptimo» en un acuario que alberga muchas especies. Aún el pH del agua de mar (8.0 a 8.3) podría ser sub-óptimo para algunas de sus criaturas, pero se determinó hace más de 8 años que niveles de pH diferentes a los del agua de mar (por ejemplo menos de 7.3) estresan a los peces. Información adicional existe ahora acerca de los rangos de pH óptimos para muchos organismos, pero los datos son completamente inadecuados para permitir a los acuaristas optimizar el pH para la mayoría de los organismos que les interesan.
Adicionalmente, los efectos del pH sobre los organismos pueden ser directos o indirectos. La toxicidad de los metales tales como cobre y níquel para algunos de los organismos del acuario, tales como, mísidos (Mysidopsis bahia) y anfípodos, se sabe que cambia con el pH. Consecuentemente, el rango aceptable de pH en un acuario puede variar con respecto a otros, aún si contiene los mismos organismos, pero tienen diferentes concentraciones de metales.
Cambios en el pH sin embargo, impactan substancialmente algunos procesos fundamentales que tienen lugar en organismos marinos. Uno de estos procesos fundamentales es la calificación, o deposición de carbonato de calcio en los esqueletos, que se sabe dependen del pH, cayendo conforme el pH baja. Usando este tipo de información, junto con la experiencia de los acuaristas, podemos desarrollar unas guías acerca de lo que son los rangos de pH aceptables en el acuario de arrecife, y que valores se salen del límite.
El rango aceptable de pH para los acuarios de arrecife es una opinión más que un hecho definido, y variará con la opinión de quien la proporciona. Este rango puede también ser bastante diferente de «rango óptimo»Sin embargo, justificar qué es óptimo, es más complicado que justificar qué es simplemente aceptable, por lo que nos enfocaremos en lo último. Como meta, sugiero el pH del agua de mar, alrededor de 8.2 como apropiado, pero el acuario de arrecife puede claramente prosperar en un rango amplio de valores de pH. En mi opinión, un rango de pH entre 7.8 y 8.5 es un rango aceptable para el acuario de arrecife, con varias consideraciones. Estas son:
-
Que la alcalinidad sea al menos 2.5 meq/L, y preferiblemente alta en el punto bajo de esta escala de pH. Baso este comentario parcialmente en el hecho de que muchos acuarios de arrecife operan efectivamente en el rango de pH de 7.8 a 8.0, y que muchos de los mejores ejemplos de estos tipos de acuario incorporan reactores de carbonato de calcio/dióxido de carbono que, mientras que tienden a bajar el pH, mantiene el nivel de alcalinidad bastante alto (mayor a 3 meq/L.). En este caso, cualquier problema asociado con calcificación a estos niveles bajos de pH pueden ser solucionados gracias a la alta alcalinidad.
-
Que el nivel de calcio sea al menos 400 ppm. La calcificación se vuelve más difícil conforme el pH y los niveles de calcio bajan. No es deseable forzar al extremo pH, calcio y alcalinidad al mismo tiempo, así que si el pH es bajo y no puede cambiarse fácilmente (como puede ser el caso en un acuario con un reactor de CaCO3/CO2), al menos asegúrense que el nivel de calcio es normal o alto (~400-450 ppm).
-
De igual forma, uno de los problemas a pH elevado (cualquier valor arriba de 8.2, pero progresivamente más problemático con cada incremento) es la precipitación abiótica del carbonato de calcio, resultando en una caida en el calcio y alcalinidad, y el taponado de los impellers de las bombas y los calefactores. Si mandan el pH a 8.4 o mayor (como ocurre a menudo cuando se usa agua de cal), asegúrense de que ambos, el calcio y la alcalinidad son mantenidos adecuadamente (eso es, ni muy bajo, inhibiendo la calcificación, ni muy elevado, causando la precipitación abiótica sobre el equipo).
-
Peaks transitorios elevados, son menos dañinos que peaks transitorios hacia abajo.
La importancia primaria del magnesio es su interacción con el balance de calcio y la alcalinidad en el arrecife. El agua de mar y la del acuario están siempre supersaturadas con carbonato de calcio. Esto es, los niveles de calcio y carbonato en solución exceden la cantidad que el agua puede mantener en equilibrio. ¿Cómo puede ser? El magnesio es una gran parte de la respuesta. En cuanto el calcio comienza a precipitar, el magnesio se enlaza a la superficie de los cristales de carbonato de calcio que precipitan. El magnesio tapona efectivamente la superficie de los cristales, por lo que ya no se ve como carbonato de calcio, haciéndolo incapaz de reclutar más calcio y carbonato, por lo que la precipitación para. Sin el magnesio, la precipitación abiótica (no biológica) del carbonato de calcio podría incrementarse lo suficiente para prohibir el mantener los niveles de calcio y alcalinidad en niveles naturales.
Por esta razón, sugiero llegar a la concentración natural de magnesio en el agua de mar: ~1285 ppm. Para propósitos prácticos, 1250-1350 ppm está bien, y niveles ligeramente fuera de este rango (1200-1400 ppm) son también aceptables. No sugiero elevar el magnesio más de 100 ppm por día, en caso de que el suplemento de magnesio tenga impurezas. Si necesitan elevarlo en varios cientos de ppm, dosificarlo por varios días permitirá de manera más adecuada alcanzar la concentración deseada, y permitiría al acuario manejar cualquier posible impureza que contenga el suplemento.
Un acuario de corales y alga coralina puede acabarse el magnesio al incorporarlo en sus esqueletos de carbonato de calcio. Muchos métodos de adicionar calcio y alcalinidad podrían no proporcionar suficiente magnesio para mantener un nivel normal. Agua de calcio sedimentada (kalkwasser), en particular, es bastante deficiente en magnesio. Consecuentemente, el magnesio debe medirse ocasionalmente, en particular si el calcio en el acuario parecen difíciles de mantener. Acuarios con excesiva precipitación abiótica de carbonato de calcio sobre objetos como calentadores y bombas, pueden sufrir de niveles bajos de magnesio (junto con alcalinidad, calcio y pH alto).
















Pingback: Comenzando con el acuario – ReefKeepers